- Biển số
- OF-359543
- Ngày cấp bằng
- 23/3/15
- Số km
- 1,090
- Động cơ
- 266,381 Mã lực
BÀI SỐ 444: CẢI TIẾN THUỐC ĐÍCH EGFR THẾ HỆ 3 OSIMERTINIB
1. Song song với hướng đi tìm ra những Thuốc mới tốt hơn, hiệu quả hơn thì còn một hướng đi nữa là cải tiến những thuốc đang có sẵn để trở thành một phiên bản tốt hơn của chính nó.
Chủ đề cải tiến này mình đã bàn trên nhóm cách đây 3 tháng-trong bài đó chúng ta đã bàn về việc cải tiến Thuốc đích ALK th3 Lorlatinib.
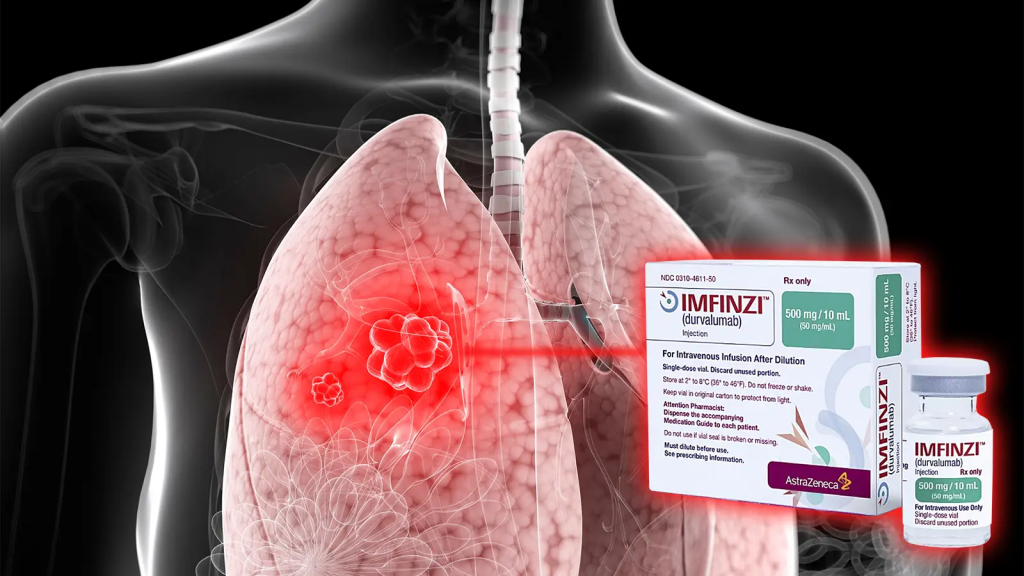
Hôm nay chúng ta trở lại chủ đề này và mục tiêu cải tiến lần này là Thuốc đích EGFR th3 Osimertinib !
2. Vào ngày 7/2/2025, Chuyên gia Baohui Han cùng các đồng nghiệp đã cập nhật kết quả ở phase1 của Thuốc Asandeutertinib. Thuốc Asandeutertinib được thiết kế là phiên bản cải tiến của Thuốc đích EGFR thế hệ 3 Osimertinib. Sự cải tiến này nhằm mong muốn đem lại hiệu quả hơn và ít độc tố hơn!
Tổng cộng 105 bệnh nhân ung thư phổi không tế bào nhỏ giai đoạn tiến triển DƯƠNG TÍNH đột biến gen EGFR EXON19 hoặc L858R đã được đưa vô nghiên cứu. Bệnh nhân trong nghiên cứu được điều trị bằng Thuốc Asandeutertinib ở liều lên thang từ 20mg cho đến 200mg một lần mỗi ngày. Kết quả phân tích cho thấy:
=>> Tỷ lệ đáp ứng khách quan đạt 85.9% và trung vị thời gian sống không bệnhh tiến triển đạt 21.5 tháng.
=>> Xét riêng phân nhóm bệnh nhân dương tính đột biến gen L858R ( được coi là đáp ứng kém hơn so với đột biến EXON19): Tỷ lệ đáp ứng khách quan đạt 86.1% và trung vị thời gian sống không bệnh tiến triển đạt 19.3 tháng.
=>> Tỷ lệ bệnh nhân mắc tác dụng phụ từ mức độ 3 trở lên là 30.5%.
Nhóm nghiên cứu kết luận:” Thuốc Asandeutertinib được cải tiến từ Thuốc đích EGFR th3 Osimertinib đã đem lại khả năng dung nạp và hiệu quả đáng kể khi điều trị cho những bệnh nhân ung thu phổi không tế bào nhỏ DƯƠNG TÍNH đột biến gen EGFR, ĐẶC BIỆT là đối với bệnh nhân dương tính L858R.”

 www.facebook.com
www.facebook.com

1. Song song với hướng đi tìm ra những Thuốc mới tốt hơn, hiệu quả hơn thì còn một hướng đi nữa là cải tiến những thuốc đang có sẵn để trở thành một phiên bản tốt hơn của chính nó.
Chủ đề cải tiến này mình đã bàn trên nhóm cách đây 3 tháng-trong bài đó chúng ta đã bàn về việc cải tiến Thuốc đích ALK th3 Lorlatinib.
Hôm nay chúng ta trở lại chủ đề này và mục tiêu cải tiến lần này là Thuốc đích EGFR th3 Osimertinib !
2. Vào ngày 7/2/2025, Chuyên gia Baohui Han cùng các đồng nghiệp đã cập nhật kết quả ở phase1 của Thuốc Asandeutertinib. Thuốc Asandeutertinib được thiết kế là phiên bản cải tiến của Thuốc đích EGFR thế hệ 3 Osimertinib. Sự cải tiến này nhằm mong muốn đem lại hiệu quả hơn và ít độc tố hơn!
Tổng cộng 105 bệnh nhân ung thư phổi không tế bào nhỏ giai đoạn tiến triển DƯƠNG TÍNH đột biến gen EGFR EXON19 hoặc L858R đã được đưa vô nghiên cứu. Bệnh nhân trong nghiên cứu được điều trị bằng Thuốc Asandeutertinib ở liều lên thang từ 20mg cho đến 200mg một lần mỗi ngày. Kết quả phân tích cho thấy:
=>> Tỷ lệ đáp ứng khách quan đạt 85.9% và trung vị thời gian sống không bệnhh tiến triển đạt 21.5 tháng.
=>> Xét riêng phân nhóm bệnh nhân dương tính đột biến gen L858R ( được coi là đáp ứng kém hơn so với đột biến EXON19): Tỷ lệ đáp ứng khách quan đạt 86.1% và trung vị thời gian sống không bệnh tiến triển đạt 19.3 tháng.
=>> Tỷ lệ bệnh nhân mắc tác dụng phụ từ mức độ 3 trở lên là 30.5%.
Nhóm nghiên cứu kết luận:” Thuốc Asandeutertinib được cải tiến từ Thuốc đích EGFR th3 Osimertinib đã đem lại khả năng dung nạp và hiệu quả đáng kể khi điều trị cho những bệnh nhân ung thu phổi không tế bào nhỏ DƯƠNG TÍNH đột biến gen EGFR, ĐẶC BIỆT là đối với bệnh nhân dương tính L858R.”

CHIẾN THẮNG UNG THƯ PHỔI | Facebook
CẬP NHẬT NHỮNG TIẾN BỘ MỚI NHẤT TRÊN THẾ GIỚI VỀ UNG THƯ PHỔI.
 www.facebook.com
www.facebook.com