BÀI SỐ 251: PHẢN BIỆN VỀ VIỆC GỘP HOÁ TRỊ+ĐÍCH KHI ĐIỀU TRỊ CHO BỆNH NHÂN UNG THƯ PHỔI DI CĂN NÃO EGFR.
1. Phác đồ gộp Hoá trị+ Đích thế hệ 3 Osimertinib trong nghiên cứu FLAURA2 đã được mình bàn rất nhiều lần trên nhóm.
->Chúng ta bàn về việc phác đồ gộp này đã nhận được phê duyệt chính thức từ Cục quản lý thực phẩm và dược phẩm Hoa Kỳ FDA.
->Chúng ta bàn về việc phân nhóm bệnh nhân dương tính
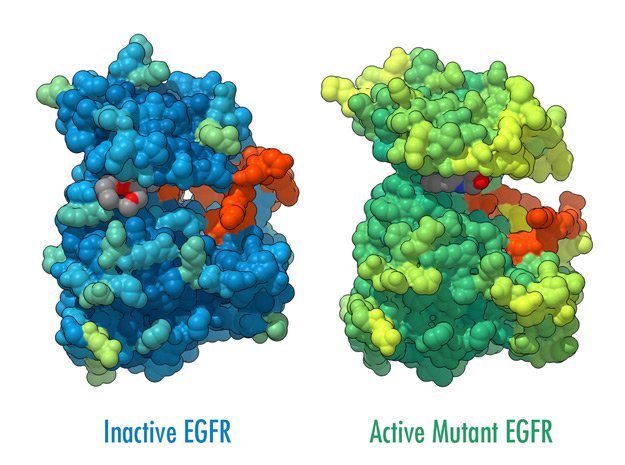
ĐỘT BIẾN GEN L858R và phân nhóm bệnh nhân
DI CĂN NÃO thực sự là 2 ứng cử viên nên ưu tiên cho phác đồ gộp.
Cái gì tồn tại thì hợp lý, cái gì hợp lý thì tồn tại. Mọi việc trên đời đều có mặt trái và mặt phải. Hai mặt trái phải này ko triệt tiêu nhau, ngược lại-chúng bổ sung cho nhau. Như mình đã từng nói rất nhiều lần trên nhóm, tất cả các nghiên cứu đều chỉ là 1 góc nhìn của nhóm chuyên gia thực hiện. Để rút ra được bài học tiệm cận gần chân lý nhất, chúng ta cần phải nhìn vấn đề từ cả góc độ ủng hộ lẫn góc độ phản biện. Chỉ khi vấn đề được mổ xẻ dưới nhiều góc độ, chân lý khi ấy mới được sản sinh.
Việc ủng hộ dùng phác đồ gộp cho di căn não chúng ta đã bàn rồi. Hôm nay, chúng ta phản biện lại góc nhìn đó!!!
2. Vào hôm 3/4/2024, Chuyên gia Yao Yu cùng các đồng nghiệp tại Trung tâm ung thư Memorial Sloan Kettering ở New York, Mỹ đã công bố báo cáo
PHẢN BIỆN về việc áp dụng phác đồ gộp Hoá Trị+ Đích khi điều trị cho bệnh nhân ung thư phổi di căn não dương tính đột biến gen EGFR.
Theo Nghiên cứu FLAURA2, việc gộp Hoá trị + Đích Osimertinib đã cải thiện đáng kể thời gian sống không bệnh tiến triển và lợi ích của việc thêm Hoá trị vô với Đích được nhận thấy rõ ràng nhất trên phân nhóm bệnh nhân được chẩn đoán mắc di căn não tại thời điểm phát hiện bệnh ( HR 0.47 ) so với phân nhóm bệnh nhân
KO mắc di căn não ( HR 0.75). Cho đến thời điểm hiện tại, dữ liệu chưa được hoàn thiện và sống còn toàn bộ chưa đạt được cải thiện có ý nghĩa về mặt thống kê ( HR 0.90, P=0.52).
Điều đáng chú ý là tỷ lệ mắc tác dụng phụ nặng từ cấp độ 3 cho tới cấp độ 5 ( tác dụng phụ được chia làm 5 cấp độ 1,2,3,4,5. Trong đó 1 là nhẹ nhất và 5 là tử vong ) của phác đồ gộp Hoá trị+ Đích
CAO HƠN RẤT NHIỀU so với phác đồ dùng Đích đơn độc, cụ thể là 64% so với 29%. Tỷ lệ tử vong gây ra bởi tác dụng phụ ở phác đồ gộp cũng cao gấp đôi khi so với phác đồ đơn độc, cụ thể là 7% so với 3%.
Với hồ sơ độc tính như vậy kèm thêm dữ liệu sống còn toàn bộ hiện chưa có, Chúng tôi
THỰC SỰ QUAN NGẠI về quan điểm của nhóm tác giả nghiên cứu FLAURA2 khi họ cho rằng:” Phác đồ gộp Hoá trị+ Đích Osimertinib nên là tiêu chuẩn chăm sóc mới và là chiến lược hợp lý để tránh tác dụng phụ trên hệ thần kinh gây ra bởi xạ trị trên nhóm bệnh nhân di căn não”.
3. Bệnh nhân ung thư phổi di căn não sẽ có sự khác biệt đáng kể về kích cỡ u di căn cũng như số lượng u di căn. Có bệnh nhân u di căn nhỏ- số lượng ít, có bệnh nhân u di căn lớn- số lượng nhiều, thậm chí có cả những bệnh nhân vi di căn màng não mềm!!
Hầu hết những bệnh nhân ung thư phổi không tế bào nhỏ EGFR mắc di căn não tại thời điểm chẩn đoán mà có tình trạng bệnh ở mức giới hạn đều có thể được điều trị hiệu quả chỉ bằng một mình Thuốc đích có kèm thêm xạ não hoặc
KO cần xạ não ( xạ phẫu ). Thực tế này cũng được ghi nhận trong chính nghiên cứu FLAURA2. Trong nghiên cứu FLAURA2, có tổng cộng 222 bệnh nhân được chẩn đoán mắc di căn não dựa trên hình ảnh phim chụp. Nếu định nghĩa bệnh có thể đo lường được là khi đường kính của khối u phải đạt trên 10mm thì chỉ có 78 bệnh nhân ( chiếm 35%) được xếp vào diện bệnh có thể đo lường.
Khi dùng Thuốc đích Osimertinib đơn độc, không có gì bất ngờ:
->Phân nhóm bệnh nhân có thể đo lường bệnh có thời gian sống không bệnh tiến triển nội sọ thấp hơn
NHIỀU khi so với phân nhóm bệnh nhân
KO thể đo lường bệnh, cụ thể là 17.3 tháng so với 27.6 tháng!
-> Phân nhóm bệnh nhân có thể đo lường bệnh cũng có tỷ lệ đáp ứng hoàn toàn di căn não thấp hơn
NHIỀU khi so với phân nhóm bệnh nhân
KO thể đo lường bệnh, cụ thể là 16% so với 43%!
Với khả năng lên não tốt của các loại Thuốc đích thế hệ mới, việc
TRÌ HOÃN XẠ NÃO đang ngày càng trở nên phổ biến. Ở nghiên cứu FLAURA2, cũng có một số ít bệnh nhân đã xạ não trước khi được tuyển vô nghiên cứu. Chúng tôi và các nhóm chuyên gia khác cũng đã từng báo cáo đầu ra sống còn rất thuận lợi với cách tiếp cận này ( Trì hoãn xạ não hoặc xạ não thay vì gộp hoá trị+đích). Trong cùng bối cảnh điều trị bước đầu giống như nghiên cứu FLAURA2, cũng đã có những nghiên cứu khác chỉ ra có 33% bệnh nhân khi được điều trị đơn độc bằng Thuốc đích Osimertinib đã đạt được mốc 2 năm sống không bệnh tiến triển nội sọ và chỉ có ít hơn 5% bệnh nhân cuối cùng phải cần đến xạ trị toàn não.
Theo kinh nghiệm của chúng tôi và những nhóm chuyên gia khác, vẫn có thể áp dụng thường xuyên chiến lược để bệnh nhân dùng
ĐƠN ĐỘC Thuốc đích Osimertinib kể cả sau khi họ đã trải qua xạ phẫu. Chiến lược này giúp trì hoãn độc tính của phác đồ gộp hoặc các phác đồ điều trị bước sau trong khi lợi ích vẫn được duy trì nhờ việc dùng Osimertinib đơn độc.
4. Độc tính mà xạ não gây ra phụ thuộc rất nhiều vào mức độ di căn, vị trí di căn cũng như kỹ thuật mà liệu pháp xạ trị áp dụng. Tiêu chuẩn chăm sóc đối với bệnh nhân di căn não chưa lan rộng là xạ phẫu. Trong nhiều thử nghiệm ngẫu nhiên phase3, xạ phẫu đều cho thấy tác dụng phụ mà nó gây ra trên hệ thần kinh ít hơn rất nhiều so với xạ toàn não. Tỷ lệ bệnh nhân mắc tác dụng phụ từ cấp độ 3 trở lên khi xạ phẫu chỉ là 2%.
Ngày nay, các tình huống phải dùng đến xạ toàn não ngày càng hiếm gặp, chưa kể việc áp dụng kỹ thuật xạ trị tránh vùng hồi hải mã và việc sử dụng thuốc Memantine đã giúp giảm thiểu đáng kể tác dụng phụ trên hệ thần kinh do xạ não gây ra. Hơn nữa, Hoá trị cũng có tác động bất lợi đến hệ thần kinh. Vì vậy, khi không có dữ liệu chi tiết về nhận thức thần kinh trong nghiên cứu FLAURA2, sẽ
RẤT KHÓ có thể biết được việc gộp thêm Hoá trị vô với Đích Osimertinib có mang lại kết quả nhận thức thần kinh tốt hơn hay xấu đi khi so với việc dùng đơn độc Đích Osimertinib???
CẬP NHẬT NHỮNG TIẾN BỘ MỚI NHẤT TRÊN THẾ GIỚI VỀ UNG THƯ PHỔI.

www.facebook.com

 www.facebook.com
www.facebook.com


 www.facebook.com
www.facebook.com